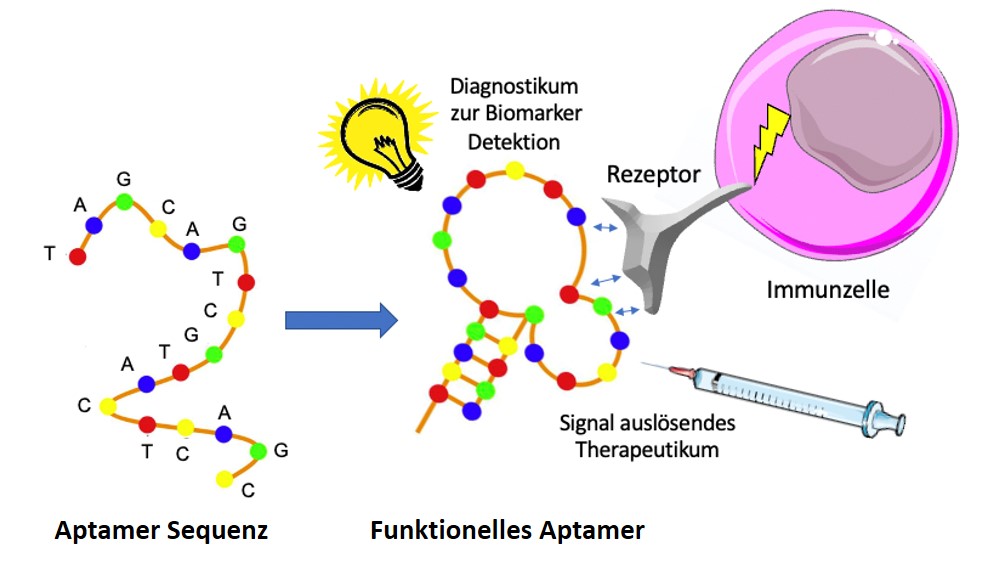
Die Plattform »Aptamere/Tolerogene Proteinkomplexe« hat das Ziel, institutsübergreifende Strukturen und Netzwerke für die Erforschung und Weiterentwicklung von MHCII-Glykopeptid-Komplexen zur Behandlung der rheumatoiden Arthritis (RA) und von Aptameren für die Nutzung zur Früherkennung von Glykosylierungsdefekten bei Autoimmunerkrankungen oder deren Vorstufen zu schaffen.
Behandlungsoptionen für die dauerhafte Krankheitskontrolle nötig
Für (auto-) immunvermittelte Erkrankungen wie der RA besteht ein großer Bedarf an neuen Therapieoptionen. Mit verfügbaren Behandlungsoptionen wie etwa Zytokinblockern wird nur selten eine Remission oder gar Heilung der Erkrankung erreicht. Gleichzeitig werden diese Erkrankungen oft erst nach Manifestation z.T. irreversibler Schädigungen diagnostiziert. Es besteht daher ein großer Bedarf an neuen Methoden zur Früherkennung und an Behandlungsoptionen zur dauerhaften Kontrolle der krankheitsunterhaltenden Autoimmunität.
Vorarbeiten
In aufwändigen Vorarbeiten wurde bereits ein rekombinanter Komplex bestehend aus dem MHC II (DRA / DRB1 * 0401) Molekül und einem galaktosylierten Collagen-II-Peptid als antirheumatische Wirksubstanz entwickelt und dessen immunregulatorisches Potenzial in einer Vielzahl präklinischer Daten belegt. Gleichzeitig wurden Methoden zur Glykanisolation und der Synthese biotinylierter Glykanstrukturen etabliert, die für die Selektion von Aptameren verwendet werden können.
Optimierung der Formulierung und Glykosylierung der MHC-II-Komplexe
Hauptziele des Projekts sind die Optimierung der Formulierung und Glykosylierung der MHC-II-Glykopeptid-Komplexe, deren Untersuchung in einem humanisierten Mausmodell der RA und die Identifizierung von Aptameren für die Entwicklung eines Detektionssystems für Glykosylierungsveränderungen.
 Fraunhofer Cluster of Excellence Immune-Mediated Diseases
Fraunhofer Cluster of Excellence Immune-Mediated Diseases