Zell- und Gentherapien sind innovative Behandlungsmethoden, die kurative Ansätze für schwere, bisher nicht heilbare Krankheiten ermöglichen. Neben der hämatopoetischen Stammzelltransplantation wurden in den letzten Jahren auch Therapien mit genetisch modifizierten Zellen als Arzneimittel für neuartige Therapien (ATMPs) in den USA und Europa zugelassen. Diese CAR-T-Zelltherapien, bei welchen patienteneigene T-Zellen mit chimären Antigenrezeptoren (CAR) modifiziert werden, finden bisher fast ausschließlich in der Krebstherapie Anwendung.
CAR-T-Zelltherapie
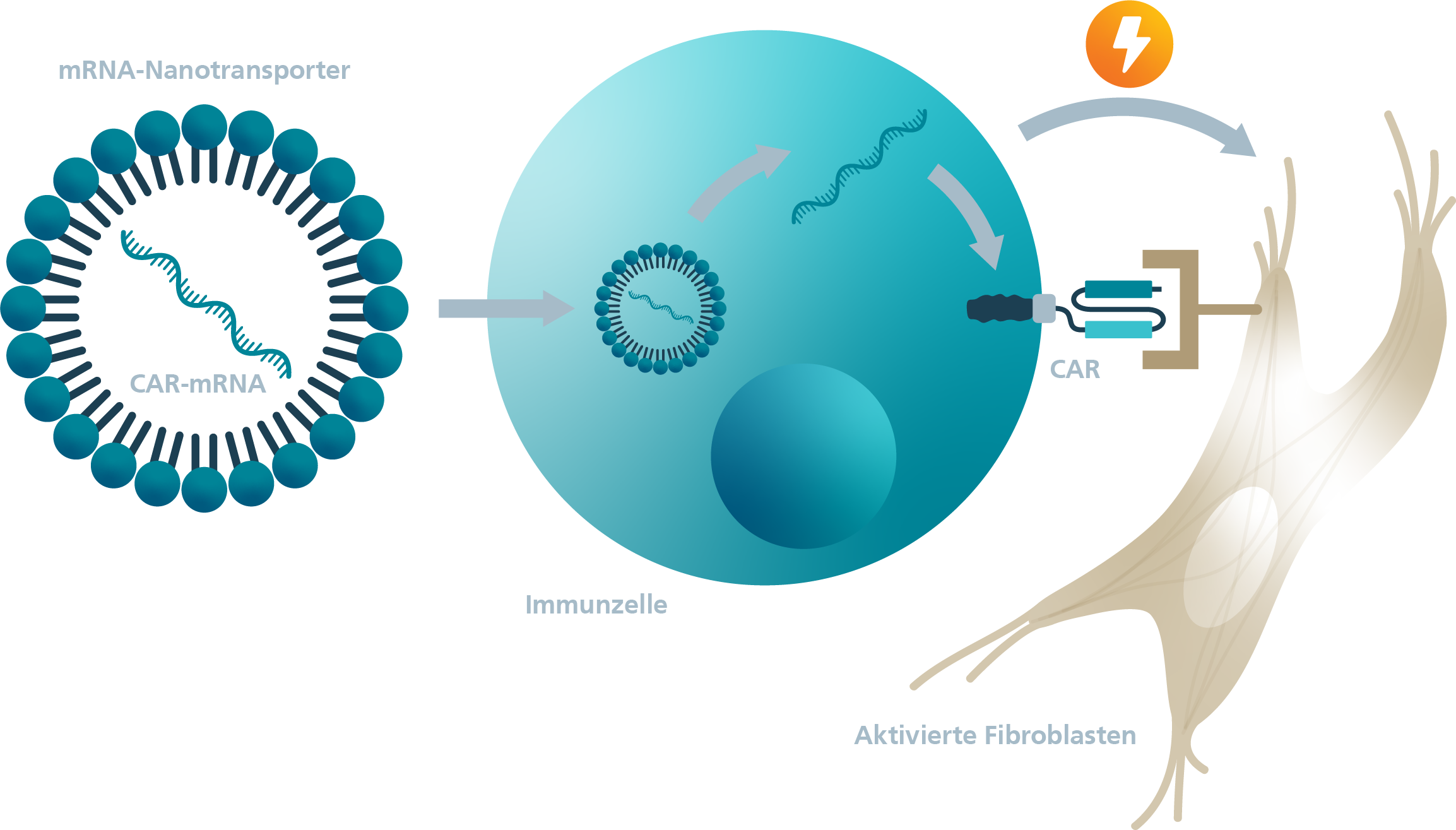
Zugelassene CAR-T-Zelltherapeutika wie auch die große Mehrheit sich in Entwicklung befindlicher, neuer CAR-T-Zellen basieren auf der stabilen gentechnischen Modifizierung patienteneigener Zellen mittels viraler Vektoren. Da die CAR-T-Zelltherapie eine sehr junge Methode ist, sind die Langzeitfolgen durch beispielsweise Off-Target-Effekte wenig untersucht. Des Weiteren kommt es durch persistente CAR-T-Zellen zu starken Nebenwirkungen. Eine Alternative zur stabilen Veränderung ist die vorübergehende Modifikation von Zellen mittels einer für das CAR-Protein kodierenden Boten-RNA (mRNA).
Ein Transfer des Therapieansatzes der CAR-T-Zelltherapie auf Infektionskrankheiten, Autoimmunerkrankungen und Fibrose ist Stand der gegenwärtigen Forschung. Bei fibrotischen Erkrankungen spielt die Stroma-Immunzell-Achse eine entscheidende Rolle. Daher stellen aktivierte, fehlgeleitete Fibroblasten ein wichtiges Ziel für die Therapien dar. Stabil erzeugte CAR-T-Zellen gegen aktivierte Fibroblasten konnten in präklinischen Studien erfolgreich zur Reduzierung von Fibrose eingesetzt werden.
 Fraunhofer Cluster of Excellence Immune-Mediated Diseases
Fraunhofer Cluster of Excellence Immune-Mediated Diseases